Par Thérèse Encrenaz
A propos de l’auteur [1]
1. INTRODUCTION
La molécule d’eau est constituée de 2 atomes – H et O – qui sont eux-mêmes très abondants dans l’Univers. C’est donc sans grande surprise que l’on trouve la molécule d’eau présente partout dans l’Univers, depuis les galaxies éloignées jusqu’aux planètes du système solaire. Sur la Terre, la molécule d’eau a la particularité unique d’être présente dans ses trois phases, solide, liquide et vapeur. Si toute l’eau contenue dans les océans et les glaciers se transformait en vapeur, nous aurions une pression atmosphérique de surface de plus de cent fois supérieure à la pression actuelle. De même, si le gaz carbonique actuellement piégé dans les océans sous forme de carbonate de calcium était relâché dans l’atmosphère, la pression augmenterait de deux ordres de grandeur, pour être comparable à celle actuellement observée à la surface de Vénus. L’atmosphère primitive de la Terre était donc très dense, et la Terre a gardé intact, sous forme essentiellement liquide, son réservoir d’eau initial. C’est ce qui lui a permis de conserver un effet de serre modéré et des conditions de température et de pression compatibles avec l’apparition et le développement de la vie.
La vie existe-t’elle dans l’Univers ? Le débat a été relancé au cours des dix dernières années avec la découverte de planètes extrasolaires (aussi appelées exoplanètes) en nombre toujours croissant. A ce jour, plus de 160 exoplanètes ont été détectées autour d’étoiles proches de type solaire. La vie peut-elle exister sur l’une d’entre elles ? Puisqu’il apparaît que l’eau – et en particulier l’eau liquide – a joué un rôle essentiel dans l’émergence de la vie, il est naturel de s’intéresser tout particulièrement à la recherche de l’eau dans l’Univers.
2. LA MOLECULE D’EAU
L’atome d’oxygène doté de deux valences disponibles, s’associe à deux atomes d’hydrogène, dotés chacun d’une valence, pour former la molécule H2O, stable et électriquement neutre. L’ensemble des réactions chimiques formant la molécule d’eau à partir des atomes O et H est parmi les plus exothermiques qui soient. Cette propriété est importante, car elle rend possible la formation de H2O dans le milieu interstellaire, à basse température, sans nécessiter la présence d’une source d’énergie externe. Sur la Terre, vis-à-vis de la photodissociation par le rayonnement UV solaire, la durée de vie de la molécule d’eau est de 36 heures (la durée de vie étant définie comme le temps nécessaire pour que le nombre de molécules soit diminué d’un facteur 2). Du point de vue thermique, la molécule d’eau est stable jusqu’à des températures de l’ordre de 3000°C.
.
Figure 1 : Structure de la molécule d’eau H2O, électriquement polarisée.
.
3. LE DIAGRAMME DE PHASE DE L’EAU
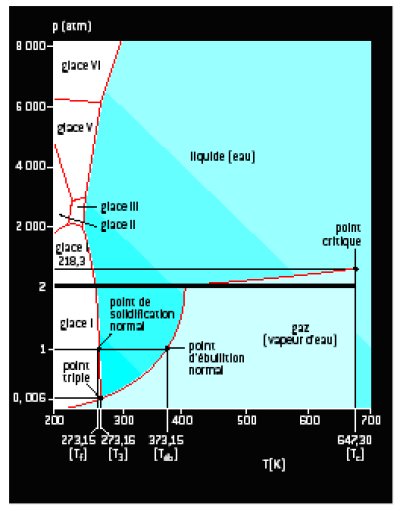
La figure 2 montre les domaines de température et de pression où l’eau se trouve à l’état gazeux, liquide ou solide. Le point triple se situe à T = 273,16 K et P = 0.006 atm. Fait remarquable, la frontière entre les états solide et liquide est pratiquement verticale dans un large domaine de pression, correspondant à une température quasiment constante et proche de celle du point triple.
La glace d’eau peut présenter différents types de structure cristalline, en fonction de la température et de la pression. Sur la Terre, on la trouve sous forme de réseau cristallin hexagonal. Entre 200 et 135 K, elle est sous forme de réseau cubique . Aux températures inférieures à 135 K, elle est amorphe ; c’est la forme la plus répandue dans le milieu interstellaire. A basse pression, l’eau interstellaire est aussi présente sous forme de vapeur. Il n’y a que sur la Terre que l’on trouve l’eau sous forme liquide. La figure 2 montre où on pourrait espérer la trouver dans les astres : (1) dans des milieux de température comprise entre 273 et 400 K, à des pressions comprises entre 0.006 et 2 bars : c’est le domaine des planètes telluriques et des éventuelles exoterres ; (2) à haute température et haute pression : c’est le domaine des intérieurs des satellites des planètes géantes.
.
Figure 2 : Le diagramme de phase de l’eau. Noter la rupture d’échelle à 2 bars sur l’axe des pressions. D’après T. Encrenaz, 2004
.
4. L’ABONDANCE DE L’EAU DANS L’UNIVERS
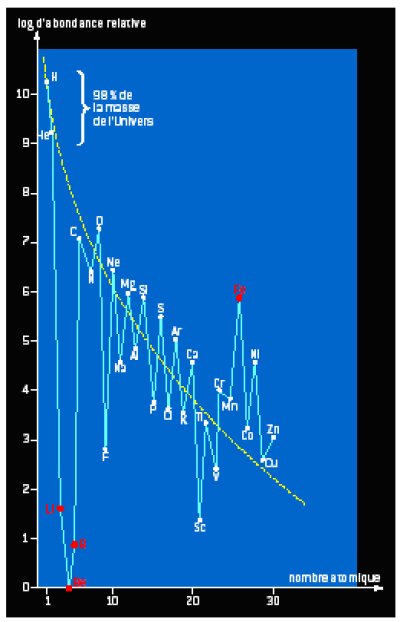
Dans l’Univers, les éléments chimiques sont d’autant plus abondants que leur masse atomique est faible. L’hydrogène, avec environ 75% de la masse totale, est le plus abondant. Vient ensuite l’hélium, avec 23%. Les deux éléments, produits directs du Big Bang, ont été formés lors de la nucléosynthèse primordiale. L’ensemble des éléments plus lourds constitue les 2% restants de la masse. Ils ont été synthétisés dans les étoiles, à commencer par les plus abondants d’entre eux, le carbone, l’oxygène et l’azote. On voit (Figure 3) que l’oxygène est l’élément le plus abondant après l’hydrogène et l’hélium.
.
Figure 3 : Courbe d’abondance des éléments chimiques dans l’Univers. D’après C. Allègre, 1985.
.
Comme l’hydrogène est de loin l’élément le plus abondant, la molécule H2O se forme dans le milieu interstellaire à partir de réactions faisant intervenir H et H2. L’ionisation de H et de H2 par les rayons cosmiques conduit à la formation de l’ion H3+. Celui-ci réagit avec l’oxygène atomique O pour former OH+ et H2, puis H2O+ et H. L’ion H2O+ réagit avec des électrons libres pour former le radical OH et la molécule neutre H2O. Dans les nuages moléculaires denses et froids, où la température n’excède pas quelques dizaines de K, la molécule d’eau peut se former directement sous forme de glace, par des réactions chimiques intervenant à la surface des grains, carbonés et/ou silicatés. La grande mobilité des atomes d’hydrogène sur les surfaces froides favorise les réactions chimiques et la formation des molécules H2O, CH4 et NH3.
5. L’OBSERVATION DE L’EAU DANS L’UNIVERS
On étudie les molécules présentes dans les astres au moyen de leur spectre électromagnétique qui porte la signature des différents éléments (atomes, ions ou molécules) qu’ils contiennent. La molécule d’eau présente trois modes normaux de vibration, tous dans le domaine infrarouge, l’un situé à 6,27 µm et les deux autres à 2,66 et 2,73 µm respectivement. De plus, de nombreuses transitions de rotation sont présentes dans l’infrarouge lointain, entre 20 et 80 µm.
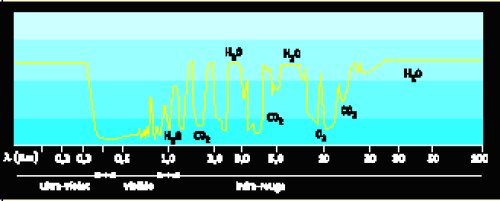
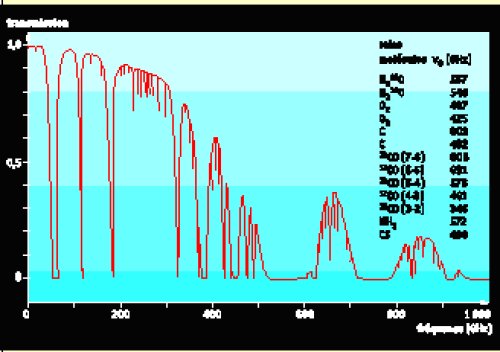
Il est très difficile de rechercher l’eau des astres directement depuis la surface de la Terre, car le rayonnement infrarouge provenant de l’extérieur est absorbé, dans la quasi-totalité du domaine infrarouge, par la vapeur d’eau présente dans l’atmosphère terrestre (Fig. 4). Il n’existe que quelques rares fenêtres d’observation, situées respectivement dans les bandes J (1,25 µm), H (1,65 µm), K (2,2 µm), L (3,5 µm), M (4,5 µm) et N (8-12 µm). Dans le domaine millimétrique, il existe également quelques fenêtres étroites accesibles à l’observation (Fig. 5). Ces domaine spectraux sont exempts de signature spectrale due à H2O, et ne sont donc pas utilisables pour rechercher la vapeur d’eau dans l’Univers. Il existe cependant une méthode qui consiste à utiliser l’effet Doppler des astres, qui décale la fréquence observée d’une raie spectrale par rapport à sa fréquence au repos ; l’effet Doppler est d’autant plus fort que la vitesse radiale est grande. Le décalage se fait vers les basses fréquences (c’est-à-dire vers le rouge) si l’objet s’éloigne. Cette méthode, fréquemment utilisée en radioastronomie, a permis en particulier la première détection de la vapeur d’eau dans une galaxie éloignée (Casoli et al., 1994).
.
Figure 4 : Absorption de l’atmosphère terrestre depuis l’UV jusqu’à l’IR lointain. Une absorption de 1 signifie que l’atmosphère est totalement opaque. Quand elle est proche de 0 (c’est le cas du domaine visible), l’atmosphère est transparente.
.
Figure 5 : Transmission de l’atmosphère terrestre dans le domaine radio, milimétrique et submillimétrique, vue depuis un site à haute altitude. Quand la transmission est proche de 1, l’atmosphère est transparente. Parmi les meilleurs sites astronomiques, on trouve le sommet du Mauna Kea (Hawaii) et le désert d’Atacama au Chili.
.
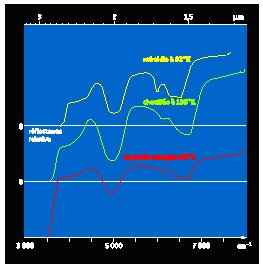
Enfin, il est possible d’observer la glace d’eau dans l’Univers depuis les télescopes au sol, car les signatures spectrales de la glace ne correspondent pas à celles de la vapeur d’eau. En l’absence de cirrus dans l’atmosphère terrestre, il est possible de rechercher dans les astres les signatures présentes à 1,5 µm, 2,0 µm et 3,1 µm, particulièrement intenses (Fig. 6).
.
Figure 6. Le spectre de la glace d’eau dans l’infrarouge proche
.
6. L’EXPLORATION DE L’EAU DANS L’UNIVERS AVEC LE SATELLITE ISO
Malgré les efforts faits pour rechercher l’eau (solide ou gazeuse) dans l’Univers depuis la Terre, il est apparu clairement que des observations étaient nécessaires en orbite autour de la Terre, de façon à s’affranchir de l’absorption atmosphérique terrestre. Tel était l’objectif du satellite européen ISO (Infrared Space Observatory) lancé par l’ESA en novembre 1995 (Kessler, 1999). Ce satellite, constitué d’une télescope de 60 cm refroidi à l’hélium liquide et de quatre intruments focaux (caméra, photomètre, spectromètres) a opéré avec succès jusqu’en mai 1998, juqu’à épuisement de sa réserve d’hélium. La première grande découverte de ISO a été la mise en évidence de l’ubiquité de l’eau dans l’Univers, sous ses formes solide et gazeuse (Encrenaz et Cox, 2000). On a trouvé la vapeur d’eau dans le milieu interstellaire (Cernicharo et al ., 1999), dans l’environnement des étoiles jeunes (Van Dishoek et al., 1999), dans l’enveloppe circumstellaire des étoiles en fin de vie (Tsuji et al., 1999), ainsi que dans les galaxies éloignées (Cox et al., 1999). Les observations du système solaire avec ISO ont également été fructueuses, avec la première détection d’une source d’oxygène dans le système solaire extérieur (Feuchtgruber et al., 1997), et le suivi de l’activité de plusieurs comètes dont Hale-Bopp (Crovisier et al., 1997). Par ailleurs, l’observation de la glace d’eau interstellaire avec ISO a montré que celle-ci n’était pas seulement sous forme amorphe (comme on le croyait auparavant), mais qu’elle pouvait également être présente sous forme cristalline (Cox et al., 1999), ce qui fixe des contraintes importantes sur les conditions de sa formation.
Notons enfin qu’à la surprise générale, on avait déjà trouvé, dès 1994, de la vapeur d’eau dans les taches solaires (Wallace et al., 1995). Son origine reste mal comprise. Peut-être est-ce le résidu de l’eau apportée par les nombreuses comètes rasantes qui sont happées par le Soleil ; le satellite SOHO en a dénombré plus d’une centaine par an.
7. CONCLUSION : LA RECHERCHE DE L’EAU DANS LES EXOPLANÈTES
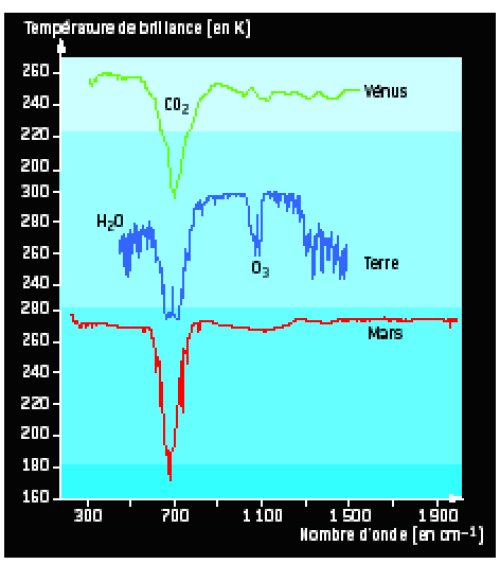
La présence généralisée de l’eau dans l’Univers permet d’envisager avec optimisme les recherches futures qui viseront à détecter l’eau des exoterres, sous forme vapeur mais aussi peut-être liquide, lorsque celles-ci (si elles existent) deviendront observables. Une méthode naturelle consistera à observer les spectres des exoterres dans l’infrarouge moyen, comme on envisage de le faire avec la mission Darwin, en préparation à l’ESA. Comme le montre la figure 7, le spectre de la Terre, comparé à celui de Vénus et de Mars, montre clairement la présence de quantités abondantes de vapeur d’eau autour de 6 µm et au-delà de 20 µm, ainsi que la signature caractéristique de l’ozone (signature vraisemblable de l’apparition de la vie sur une planète) à 9,5 µm.
.
Figure 7 . Le spectre infrarouge des planètes telluriques, entre 300 cm-1 (33 µm) et 1900 cm-1 (5,2 µm). D’après R. Hanel et al., 1992.
.
8. RÉFÉRENCES
- C. Allègre, De la pierre à l’étoile, Fayard, 1985
- F. Casoli et al., Astron. Astrophys. 287, 716, 1994
- J. Cernicharo et al., ESA SP-427, 565, 1999
- P. Cox et al., ESA SP-427, 631, 1999
- J. Crovisier et al., Science, 275, 1904, 1997
- T. Encrenaz, A la recherche de l’eau dans l’Univers, Belin, 2004
- T. Encrenaz et P. Cox, L’eau dans l’Univers, CRAS 1, IV, 981, 2000
- H. Feuchtgruber et al., Nature389, 159, 2003
- R. Hanel et al., Exploration of the solar system by infrared remote sensing, cambridge University Press, 1992
- M. Kessler, ESA SP-427, 23, 1999
- T. Tsuji et al., ESA SP-427, 229, 1999
- E. Van Dishoek et al., ESA SP-427, 579, 1999
- L. Wallace et al., Science 268, 1155, 1995
_______________________________________






Aucun commentaire sur l'article L’eau dans l’univers