En chimie, les synthèses qui utilisent des produits achiraux sont symétriques, c’est-à-dire que lorsque des composés asymétriques sont formés, ils sont racémiques. En biochimie, les composés élémentaires que sont les acides aminés et les sucres ne sont utilisés que selon une seule de leur configuration pour la synthèse de polymères biologiques (protéine ou ADN). A part de rares exceptions, la configuration L est utilisée pour les acides aminés et D pour les sucres. Cette différence entre les systèmes chimiques abiotiques et biotiques caractérise la nature homochirale de la biochimie, ce qui est une spécificité des organismes vivants, au moins sur Terre, et pourrait être considérée comme un indice pour la recherche de vie extraterrestre. C’est pourquoi, un des principaux objectifs de la chimie prébiotique est de comprendre quelle a pu être la transition entre les systèmes symétriques représentés par la chimie abiotique, et les systèmes asymétriques d’origine biochimique. Bien que les systèmes vivants présentent d’autres propriétés que celle de l’homochiralité, il n’en reste pas moins que l’émergence de biomolécules caractérisées par cette asymétrie à partir de systèmes achiraux représente une étape importante dans l’émergence de la vie.
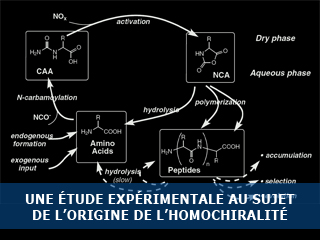
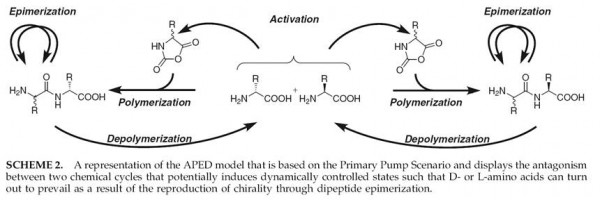
Dans un article qui vient de paraître dans la revue Astrobiology, une équipe de chercheurs Français présente une étude expérimentale de réactions chimiques qui associées entre elles pourraient mener théoriquement un pool de matière organique initialement achirale vers l’émergence d’une asymétrie et permettre l’amplification de celle-ci pour aboutir à l’homochiralité. Les réactions étudiées proviennent d’un système expérimental développé par Commeyras et al. « la Pompe Primaire » qui permet l’activation d’acides aminés pour aboutir à la formation d’oligopeptides. La répétition des cycles d’activation et de polymérisation permet à terme une accumulation de peptides dans le milieu et un recyclage de ceux-ci sous forme de peptides plus cours ou d’acides aminés. A partir de ce réacteur chimique, R. Plasson et al. ont étudié à travers une approche théorique la possibilité d’utiliser de tel réacteur pour obtenir une rupture de symétrie et son amplification par succession de cycle d’activation, de polymérisation, d’épimérisation et de dépolymérisation (APED). Dans ce schéma théorique, les réactions de polymérisation, d’épimérisation et de dépolymérisation sont présentées comme stéréosélectives et pourraient dans certaines conditions permettre une amplification d’une asymétrie d’origine aléatoire ou autre.
L’objectif des auteurs a été d’étudier expérimentalement l’épimérisation de résidus N-terminaux de dipeptides et de tripeptides ainsi que la réaction de dépolymérisation de ces oligopeptides. Il est ressorti que pour les peptides étudiés, l’épimérisation nécessite un catalyseur (pyridoxal) et que les espèces hétérochirales sont les plus stables à l’équilibre thermodynamique, et d’autant plus que le résidu C-terminal est encombré. Les espèces homochirales tendent à être plus stables sur les tripeptides par rapport aux dipeptides. En ce qui concerne la dépolymérisation, les dipeptides et tripeptides hétérochiraux se clivent plus rapidement pour mener à la formation de dicétopipérazine. Cette réaction est donc stéréosélective.
Pour en savoir plus :
Danger, G., Plasson, R., and Pascal, R. (2010) An experimental investigation of the evolution of chirality in a potential dynamic peptide system: N terminal epimerization and degradation into diketopiperazine, Astrobiology, 10, 651-662. DOI: 10.1089/ast.2009.0450



Aucun commentaire sur l'article Nouvelle étude expérimentale au sujet de l’origine de l’homochiralité