Comment l’environnement hydrothermal de la Terre Primitive a pu influencer le choix du furanose plutôt que du pyranose comme sucre constitutif de l’ADN et de l’ARN.
L’acide ribonucléique (ARN) et l’acide désoxyribonucléique (ADN) sont à la base du fonctionnement de tous les êtres vivants. Ce sont de longues chaines de nucléotides, chaque nucléotide étant formé d’un phosphate, d’une base azotée (adénine, guanine, cytosine et uracile, pour l’ARN, ou thymine, pour l’ADN) et d’un sucre, le ribose pour l’ARN et le désoxyribose (dérivé du ribose) pour l’ADN.
Le ribose utilisé par le vivant est le D-ribose (D signifiant dextrogyre[1]), de formule brute C5H10O5. Le D-ribose existe sous 5 formes, une forme linéaire et quatre formes cycliques (anomères) : le a-D-ribofuranose (aF), le b-D-ribofuranose (bF), le a-D-ribopyranose (aP), et le b-D-ribopyranose (bP). Dans l’eau, à température et pression ambiantes, ces 5 formes coexistent sous forme d’un mélange composé à 6,5% de aF, à 13,5 % de bF, à 21,5% de aP, et à 58,5% de bP [1]. Le bF ne représentant que 13,5% du mélange, il est surprenant d’observer que c’est sur cette forme que l’ARN est basé plutôt que sur un sucre de type pyranose, de loin plus stable. Dans le cadre des recherches conduites dans le domaine de la chimie prébiotique, et notamment celles s’intéressant au scénario du « monde ARN », comprendre pourquoi cet anomère a été choisi plutôt qu’un autre est donc crucial.
Il existe de nombreuses causes possibles à cette sélection préférentielle, telles que des processus chimiques spécifiques durant la phosphorylation ou la glycosylation nécessaires à la formation des nucléotides. Les conditions physicochimiques sur la Terre primitive pourraient également être responsables de l’augmentation de la concentration en furanose. En effet, lorsque la vie est apparue sur Terre il y a plus de 4 milliards d’années, l’environnement était très différent de celui d’aujourd’hui. En particulier les océans étaient beaucoup plus chauds avec des températures de l’ordre de 60°C [2]
C’est cette deuxième piste qu’une équipe de chercheurs Français et Suisses explorent dans leur article intitulé «Equilibrium and non-equilibrium furanose selection in the ribose isomerisation network» [3]. Basant leur étude sur des mesures expérimentales en spectroscopie de Résonnance Magnétique Nucléaire (RMN)[2], et sur des calculs de physique statistique, ils ont pu mettre en évidence une inversion de population entre le bF et le bP avec l’augmentation de la température. De plus, alors que cette inversion intervient autour de 156°C dans l’eau pure, elle intervient à seulement 134°C dans une eau dont la composition reproduit la composition de l’océan à l’Hadéen[3] (Fig. 1). Bien que cette température puisse sembler élevée, elle correspond à des températures observables au niveau des systèmes hydrothermaux, des lieux justement considérés comme des endroits privilégiés d’apparition de la vie [2].
Plus intéressant encore, dans cette étude les chercheurs montrent que la fraction molaire en bF peut être augmentée lorsque le système est soumis à un gradient de température, c’est-à-dire un environnement dans lequel existe un côté « chaud » et un côté « froid ». En effet, ce dernier crée un état stationnaire de non-équilibre qui peut favoriser la sélection du bF en dissipant de manière optimale l’énergie thermique fournie par le gradient. Ainsi, ils montrent que le pourcentage de furanose est de l’ordre de 47% dans un gradient de température s’étalant entre 60°C et 160°C ; un pourcentage atteint pour une température de l’ordre de 170°C dans le cas d’un système à l’équilibre. Là encore, sur une Terre primitive extrêmement active sur le plan volcanique, de tels gradients existaient très probablement à proximité des systèmes hydrothermaux sous-marins où les fluides émanant des évents percolaient à travers les sédiments adjacents, volcaniques et très réactifs.
Ces travaux proposent ainsi un modèle tangible permettant d’augmenter la concentration en furanose au-delà des limites fixées par la thermodynamique à l’équilibre. Ils permettent de décrire un scénario réaliste pouvant expliquer la sélection du furanose comme sucre de la vie à une époque où les sources hydrothermales étaient omniprésentes.
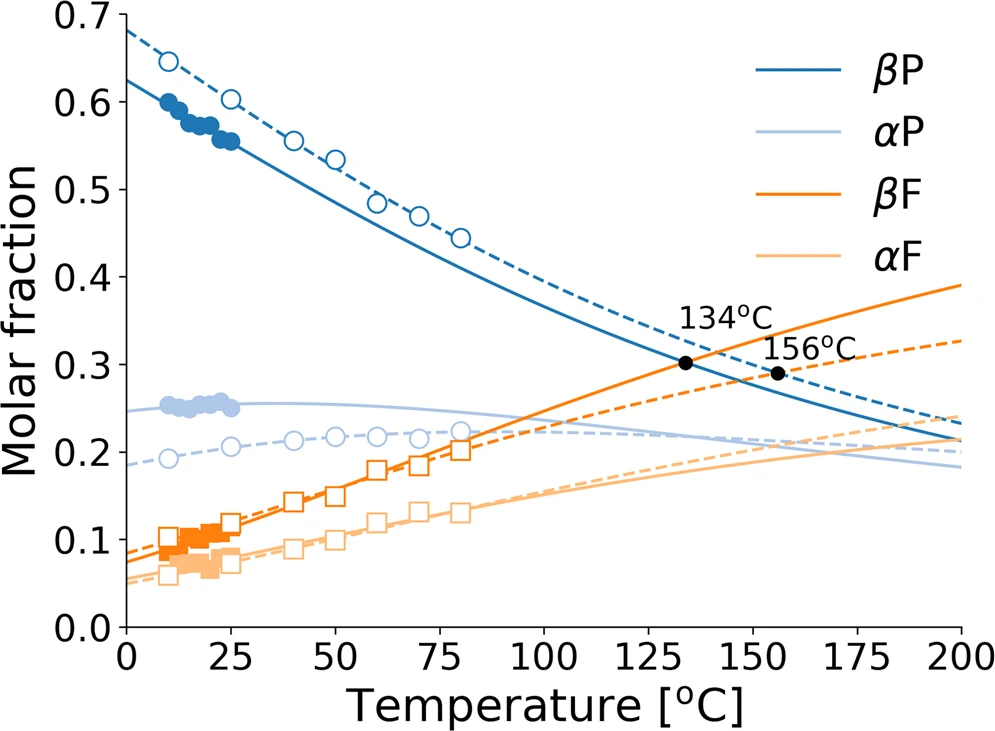
Fraction molaire des différents anomères du ribose en fonction de la température. On observe une inversion de population entre le bF et le aP pour une température de 156°C dans l’eau pure (en tirets) et pour une température de 134°C dans de l’eau « Hadéenne » (en traits pleins). aF: a-D-ribofuranose, bF : b-D-ribofuranose, aP : a-D-ribopyranose, aP : b-D-ribopyranose.
[1] Une molécule dextrogyre a la particularité de faire dévier le plan de polarisation de la lumière polarisée vers la droite. Elle s’oppose aux molécules lévogyres qui le font dévier vers la gauche. Cette propriété permet de distinguer les molécules chirales, c’est-à-dire des molécules images l’une de l’autre dans un miroir mais non superposables (comme la main gauche et la main droite par exemple).
[2] La spectroscopie RMN est une méthode qui utilise la mesure du champ magnétique autour d’un atome pour étudier sa structure et ses groupes fonctionnels, permettant ainsi l’identification de composés organiques monomoléculaires.
[3] L’Hadéen est le premier éon géologique de la Terre s’étendant -4.6 milliards d’année à, à peu près, -4 milliards d’années.
Références :
[1] K. N. Drew, J. Zajicek, G. Bondo, B. Bose, and A. S. Serianni, ‘13C-labeled aldopentoses: detection and quantitation of cyclic and acyclic forms by heteronuclear 1D and 2D NMR spectroscopy’, Carbohydrate Research, vol. 307, pp. 199–209, 1998.
[2] F. Westall et al., ‘A Hydrothermal-Sedimentary Context for the Origin of Life’, Astrobiology, vol. 18, pp. 259–293, 2018.
[3] A. V. Dass et al., ‘Equilibrium and non-equilibrium furanose selection in the ribose isomerisation network’, Nat Commun, vol. 12, no. 1, p. 2749, Dec. 2021, doi: 10.1038/s41467-021-22818-5.



Aucun commentaire sur l'article Chimie prébiotique : la sélection du furanose comme sucre de la vie